OncoCUP Dx – Test de diagnóstico para cáncer de origen desconocido
Visión general
OncoCUP Dx es una solución innovadora, no invasiva, precisa, rentable y validada, especialmente desarrollada para ayudar en el diagnostico del cáncer de origen desconocido así como para la confirmación del mismo. También tiene usos potenciales para la monitorización del tratamiento, pronóstico así como para la vigilancia ante recidivas.
OncoCUP Dx calcula el riesgo a partir de una puntuación que se obtiene de varios biomarcadores del paciente (principalmente marcadores tumorales así como de cierta información clínica del mismo).

Click here to download the brochure in PDF format.
Marcadores tumorales
Los marcadores tumorales son sustancias liberadas por las células tumorales, que entran al torrente sanguíneo u otros fluidos biológicos y son útiles para el diagnóstico, pronóstico y monitorización del tratamiento en diferentes tipos de cáncer.
La mayoría de los marcadores tumorales no son específicos de ningún tipo de cáncer y las diferencias entre las enfermedades benignas y malignas son cuantitativas (por ejemplo, los pacientes con tumores epiteliales tienden a tener niveles significativamente más altos de estos marcadores tumorales que los pacientes sin malignidad).
En la actualidad, existen más de 20 parámetros bien conocidos que son ampliamente considerados como marcadores de tumores, como el PSA ―relacionado con el cáncer de próstata―, el CA 15.3 ―relacionado con el cáncer de mama―, el CA 125 y la HE4 ―ambos relacionados con cáncer de ovario―, el CEA y el CA 19.9 ―ambos relacionados con diferentes tipos de cáncer gastrointestinal (cáncer colorrectal, gástrico y pancreático)―, o la NSE y la ProGRP ―ambas relacionados con el cáncer de pulmón―.
Sin embargo, hay una variedad de factores que pueden afectar la exactitud de los marcadores tumorales ya que hacen aumentar sus niveles sin presencia de malignidad. La razón principal son las enfermedades benignas, aunque también pueden afectar diferentes interferencias técnicas.
En este sentido, la Sociedad Española de Bioquímica Clínica y Patología Molecular, Comisión de Biomarcadores del Cáncer, estableció los Criterios Barcelona, 4 criterios que buscan ayudar a distinguir y valorar correctamente los resultados de los marcadores tumorales y reducir el número de Falsos Positivos (FP):
- Evaluación de las concentraciones séricas de los marcadores tumorales.
- Descarte de patologías benignas como principal fuente de falsos positivos.
- Recomendación de seguimiento si los marcadores tumorales arrojan resultados moderados (Zona Gris/Indeterminado).
- Eliminación de interferencias técnicas.
Mediciones estadísticas en pruebas de diagnóstico
Desafortunadamente, el uso de marcadores tumorales en la rutina presenta también otros problemas, tales como baja sensibilidad en etapas tempranas o inexistencia de un marcador tumoral específico para cada tumor maligno. Sin embargo, la combinación de 2 o más marcadores tumorales arroja mejores resultados, especialmente en etapas avanzadas.
En este sentido, la combinación de varios marcadores tumorales ―así como la inclusión de información de la historia clínica del paciente en los cálculos―, utilizando algoritmos complejos con múltiples variables, da como resultado una mayor sensibilidad y especificidad: eso es lo que hemos bautizado como MBDAA (del inglés, Multiple Biomarkers Disease Activity Algorithms).
La sensibilidad de un test de diagnóstico es el porcentaje de positivos reales que se identifican correctamente, y la especificidad es la proporción de negativos verdaderos que se clasifican correctamente. Ambas variables están estrechamente unidas entre sí y dan una idea de la exactitud de dicho test.
Un test que identifique correctamente todos los verdaderos positivos como positivos, pero que tenga muchos falsos negativos tendría una sensibilidad del 100%, pero una baja especificidad. Por ejemplo, la sensibilidad mide el número de tumores malignos que se identifican correctamente como cáncer, mientras que la especificidad mide el número de tumores no malignos que se identifican correctamente como benignos. Una alta sensibilidad significa menos cánceres diagnosticados como benignos y una alta especificidad significa menos tumores benignos diagnosticados como malignos.
Además, el valor predictivo positivo (VPP) es el número de verdaderos positivos correctamente identificados sobre el total de positivos reales. Una prueba con muchos falsos positivos tendrá un VPP bajo. Por otra parte, el valor predictivo negativo (VPN) es el número de negativos verdaderos correctamente identificados sobre el total de negativos reales. Un alto valor VPN significa que muy pocos positivos verdaderos fueron incorrectamente identificados como negativos.
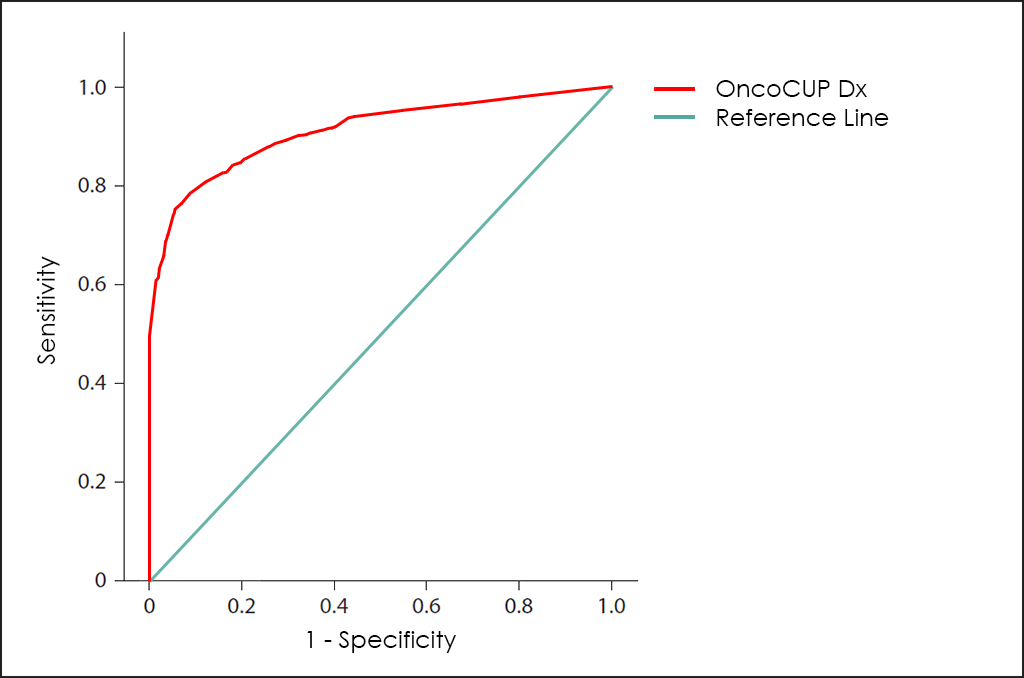
Todos estos parámetros diferentes se pueden representar juntos en un gráfico que se conoce como curva ROC (del inglés, Receiving Operator Curve), donde se muestran mejores resultados con curvas que tienden a acercarse a la esquina superior izquierda de la imagen (100% de sensibilidad y 100% de especificidad).
Curva ROC
La curva ROC del test OncoCUP Dx ―basado en el recuento combinado de los marcadores tumorales AFP, CA 15.3, CA 19.9, CA 72.4, CA 125, CEA, CYFRA 21-1, HE4, NSE, ProGRP, PSA, fPSA, SCC y S100; diferentes comorbilidades, así como otros datos de 5.456 pacientes consecutivos (ajustados posteriormente mediante hallazgos de otras investigaciones)―, muestra unas capacidades de diagnóstico realmente interesantes: 82,4% de sensibilidad y 98,1% de especificidad.
Cómo funciona
Como todos los tests MBDAA de BIOPROGNOS, OncoCUP Dx está disponible en línea a través de un acceso seguro a nuestra plataforma Cloud. Como solución en la nube, OncoCUP Dx está diseñado para ser utilizado en modalidad Software as a Service (SaaS), es decir, sin instalación, sin actualizaciones periódicas, con bajo coste total de adquisición, así como sin costes de mantenimiento.
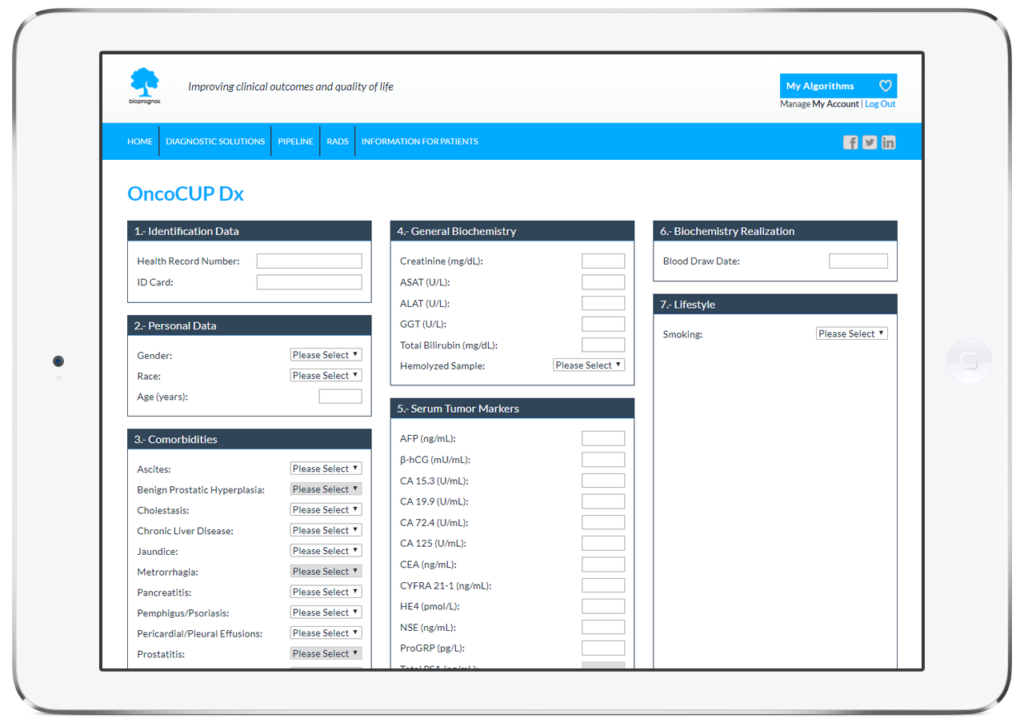
De esta manera, los doctores o los técnicos de laboratorio tan solo deben llenar el formulario online con los valores obtenidos previamente de los pacientes (datos personales, comorbilidades, valores de los marcadores tumorales así como la información de estilo de vida del paciente) y pulsar en el botón Enviar para obtener el riesgo de tener cáncer.
Hojas de pedido
Para facilitar el trabajo, los doctores pueden descargarse y re llenar el formulario de pedido del test OncoCUP Dx de una manera rápida y fácil ―con todos los datos necesarios para un cálculo óptimo del riesgo ya detallados―.

Pulse aquí para descargarse la hoja de pedido de OncoCUP Dx en formato PDF.
Informe final
Después de que los doctores introduzcan los datos del paciente en el formulario online, la aplicación presenta los resultados en una pantalla separada, permitiendo su conversión en documento PDF para ser descargado o enviado por correo electrónico.


Pulse aquí para descargarse el informe en formato PDF.
El informe incluye dos secciones principales: Información del paciente y Resultado. En la primera se muestran todos los datos del paciente introducidos previamente para su seguimiento. La segunda incluye: Resultados, que indican si los niveles de los marcadores tumorales están dentro del rango de normalidad o no; Riesgo, con una barra de puntuación que muestra la probabilidad de tener cáncer; Comentarios, creados dinámicamente para ayudar a los doctores y a los profesionales de la salud a entender de una manera fácil cómo se han detectado falsos positivos (como niveles de marcadores tumorales sospechosos de presencia de cáncer, pero que al considerar las otras variables en conjunto, no se corresponden con hallazgos malignos); y, finalmente, las Conclusiones, con recomendaciones que sugieren la presencia de cáncer, repetir el test en 4 semanas (para el riesgo moderado, es decir, aquellos casos en los que los niveles de los marcadores tumorales son superiores a la normalidad pero en los que no está claro ser de alto riesgo), o repetir el test en 1 año para los resultados de bajo riesgo.
Téngase en cuenta que el informe final está orientado tan solo para profesionales de la salud ―no para pacientes―, ya que OncoCUP Dx ha sido diseñado como “una herramienta para ayudar a los profesionales de la salud en el diagnóstico de cáncer”, y certificado con esta finalidad por la DECLARACIÓN DE CONFORMIDAD CE (Directiva de Dispositivos Médicos 93/42/CEE, Clase I, Regla 12).
Declaración de conformidad CE
Desde el pasado 17 de mayo de 2017 (cuando se lanzó la versión 1.0), OncoCUP Dx posee la Declaración de Conformidad CE que certifica que ha sido evaluado para cumplir con altos requisitos de seguridad, salud y protección ambiental.

Pulse aquí para descargarse la DECLARACIÓN DE CONFORMIDAD CE de OncoCUP Dx en formato PDF.
Esta declaración certifica la prueba OncoCUP Dx para todo el Espacio Económico Europeo (EEE).
Además, también hay otras dos ventajas importantes que otorga el marcado CE, tanto a las empresas como a los consumidores en el EEE:
- Las empresas tienen la garantía que los productos que disponen del marcado CE pueden comercializarse en todo el EEE.
- Los consumidores tienen la garantía que se dispone del mismo nivel de salud, seguridad y protección medioambiental en todo el EEE.
Usos y propósitos de OncoCUP Dx
OncoCUP Dx ha sido desarrollado para:
- Confirmar o descartar malignidad en resultados obtenidos anteriormente con otras pruebas, tales como tomografía computarizada (TC) o imágenes de resonancia magnética (IRM), gracias a una mayor sensibilidad y especificidad que los procedimientos de imagen.
- Ayudar a los doctores a predecir el comportamiento del cáncer y su respuesta al tratamiento, así como las posibilidades de recuperación de una persona.
- Guiar en las decisiones de tratamiento (ayudar a decidir si se debe añadir inmunoterapia después de la cirugía y/o radioterapia); monitorización de la terapia (los doctores pueden usar los cambios en la presencia o cantidad de uno o más marcadores tumorales para evaluar cómo el cáncer está respondiendo al tratamiento); así como predecir o monitorizar posibles recidivas (la detección de cambios en los valores de los marcadores tumorales en controles seriados puede ser parte del plan de seguimiento, lo que puede ayudar a detectar una recurrencia antes que otros métodos).
La ciencia detrás de OncoCUP Dx
Investigaciones de referencia
- Bayo J., Castaño M. A., Rivera F. and Navarro F. (2017). “Analysis of blood markers for early breast cancer diagnosis”. Clin Transl Oncol. Springer. DOI: 10.1007/s12094-017-1731-1
- Best J., Bilgi H., Heider D., Schotten C., Manka P., Bedreli S., Gorray M., Ertle J., van Grunsven L. A. and Dechêne A., “The GALAD scoring algorithm based on AFP, AFP-L3 and DCP significantly improves detection of BCLC Early Stage”. Georg Thieme Verlag KG. DOI: 10.1055/s-0042-119529
- Reichl P., Fang M., Starlinger P., Staufer K., Nenutil R., Muller P., Greplova K., Valik D., Dooley S., Brostjan C., Gruenberger T., Shen J., Man K., Trauner M., Yu J., Fang Gao C. and Mikulits W. “Multicenter analysis of soluble Axl reveals diagnostic value for very early stage HCC”. Int. J. Cancer: 137, 385–394 (2015) VC 2014 UICC. DOI: 10.1002/ijc.29394
- Molina, R., Marrades R. M., Auge J. M., Escudero J. M., Vinolas N., Reguart N., Ramirez J., Filella X., Molins L. and Agusti A. (2016). “Assessment of a Combined Panel of Six Serum Tumor Markers for Lung Cancer.” Am J Respir Crit Care Med 193(4): 427-437. DOI: 10.1164/rccm.201404-0603OC
- Molina, R., Auge J. M., Escudero J. M., Filella X., Foj, L., Torné A., Lejarcegui J., Pahisa J. “HE4 a novel tumour marker for ovarian cancer: comparison with CA 125 and ROMA algorithm in patients with gynaecological diseases.” Tumour Biol, 2011. 32(6): p. 1087-95. PMCID: PMC3195682
- Santotoribio J.D., Garcia-de la Torre A., Cañavate-Solano C., Arce-Matute F., Sanchez-del Pino M.J., Perez-Ramos S. “Cancer antigens 19.9 and 125 as tumor markers in patients with mucinous ovarian tumors.” EJGO European Journal of Gynaecological Oncology. PMID: 27048105
- Shaikh N. A., Memon F., Samo R. P. “Tumor markers; efficacy of CA-125, CEA, AFP and Beta-HCG. An institutional based descriptive & prospective study in diagnosis of ovarian malignancy.” Professional Med J 2014;21(4):621-627. PDF
- Sørensen S. S., Mosgaard B. J. “Combination of CA 125 and CEA can improve ovarian cancer diagnosis.” DANISH MEDICAL BULLETIN. Dan Med Bul 2011;58(11):A4331. November 2011. PDF
- Salami S. S., Schmidt F., Laxman B., Regan M. M., Rickman D. S., Scherr D., Bueti G., Siddiqui J., Tomlins S. A., Wei J. T., Chinnaiyan A, Rubin M. A., Sanda M. G. “Combining Urinary Detection of TMPRSS2:ERG and PCA3 with Serum PSA to Predict Diagnosis of Prostate Cancer.” Urol Oncol. 2013 July ; 31(5): 566–571. DOI: 10.1016/j.urolonc.2011.04.001
- Molina, R., Bosch X., Auge J. M., Filella X., Escudero J. M., Molina V., Sole M. and Lopez-Soto A. (2012). “Utility of serum tumor markers as an aid in the differential diagnosis of patients with clinical suspicion of cancer and in patients with cancer of unknown primary site.” Tumour Biol 33(2): 463-474. DOI: 10.1007/s13277-011-0275-1
- Trapé, J. and Molina R. (2006). “Aspectos generales de los marcadores tumorales.” JANO 1620: 45-48. PDF
- Molina R., Filella X., Trapé J., Augé J. M., Barco A., Cañizares F., Colomer A., Fernandez A., Gaspar M. J., Martinez-Peinado A., Pérez L., Sánchez M., Escudero J. M. (2013). “Principales causas de falsos positivos en los resultados de marcadores tumorales en suero.” Sociedad Española de Bioquímica Clínica y Patología Molecular. Comisión de Marcadores Biológicos del Cáncer. PDF
Otras investigaciones relacionadas
- Abdelmoniem S, Zaki E, Imam H, Badrawy H, Ali S, Maximous D. Diagnostic value of a panel of tumor markers as a part of a diagnostic work-up for ascites of unknown etiology – Open Journal of Gastroenterology – 2012. DOI: 10.4236/ojgas.2012.23020
- Briasoulis E, Pavlidis N. Cancer of Unknown Primary Origin. Department of Medicine/Oncology Unit, Ioannina University Hospital, Ioannina, Greece. The Oncologist 1997;2:142-152. DOI: 10.1.1.484.4291
- Duffy, M. J. (2010). “Clinical Utility of Tumor Markers: What the Guidelines Recommend.” Journal of Laboratory Diagnostics 46(3): 281-291. PDF
- Duffy, M. J. and P. McGing (2010). Guidelines for the use of Tumour Markers. PDF
- Fizazi K, Greco F, Pavlidis N, Daugaard G, Oien K, Pentheroudakis G. Cancers of unknown primary site: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up – Annals of Oncology – 2015. DOI: 10.1093/annonc/mdv305
- Furrukh M, Burney I.Cancer of Unknown Primary Site: Not All is Lost! JBR Journal of Clinical Diagnosis and Research – 2015. DOI: 10.4172/2376-0311.1000115
- Hemminki K, Bevier M, Hemminki A, Sundquist J. Survival in cancer of unknown primary site: population-based analysis by site and histology. Ann Oncol. 2012;23(7):1854-63. PMID: 22115926
- Hemminki K, Ji J, Sundquist J, Shu X. Familial risks in cancer of unknown primary: tracking the primary sites. J Clin Oncol. 2011;29(4):435-40. DOI: 10.1200/JCO.2010.31.5614
- Mayeux, R. (2004). “Biomarkers: potential uses and limitations.” NeuroRx 1(2): 182-188. DOI: 10.1602/neurorx.1.2.182
- Medicine, T. A. f. c. B. L. (2013). RECOMMENDATIONS AS A RESULT OF THE ACB NATIONAL AUDIT ON TUMOUR MARKER SERVICE PROVISION. PDF
- NICE Clinical Guidelines, No. 104. Diagnosis and management of metastatic malignant disease of unknown primary origin. Clinical Guideline. Evidence Review. National Collaborating Centre for Cancer (UK); 2010 Jul. PMID: 22259823
- Novakovic, S. (2004). “Tumor markers in clinical oncology.” Radiology and Oncology 38(2). PDF
- Perez, E. O. and M. I. Aceituno Azaustre (2014). “Utilidad clínica de los marcadores tumorales.” Revista Médica de Jaén(4): 2-12. PDF
- Perkins, G. L., E. D. Slater, G. K. Sanders and J. G. Prichard (2003). “Serum Tumor Markers.” American Family Physician 68(6): 1075 – 1082. PDF
- Sharma, S. (2009). “Tumor markers in clinical practice: General principles and guidelines.” Indian J Med Paediatr Oncol 30(1): 1-8. PMCID: PMC2902207
- Stieber, P., R. Hatz, S. Holdenrieder, R. Molina, M. Nap, J. von Pawel, A. Schalhorn, J. Schneider and K. Yamaguchi (2006). Practice Guidelines And Recommendations For Use Of Tumor Markers In The Clinic. National Academy of Clinical Biochemistry Guidelines for the use of tumor markers in Lung Cancer. PDF
- Sturgeon, C. (2002). “Practice guidelines for tumor marker use in the clinic.” Clin Chem 48(8): 1151-1159. PMID: 12142367
- Sturgeon, C. M., E. P. Diamandis, B. R. Hoffman, D. W. Chan, S. L. Ch’ng, E. Hammond, D. F. Hayes, L. A. Liotta, E. F. Petricoin, M. Schmitt, O. J. Semmes, G. Söletormos and E. van der Merwe (2009). National Academy of Clinical Biochemistry Laboratory Medicine Practice Guidelines for use of tumor markers in clinical practice: quality requirements. DOI: 10.1373/clinchem.2007.094144
- Sturgeon, C. M., M. J. Duffy, B. R. Hoffman, R. Lamerz, H. A. Fritsche, K. Gaarenstroom, J. M. G. Bonfrer, T. Ecke, H. B. Grossman, P. Hayes, R.-T. Hoffmann, S. P. Lerner, F. Lohe, J. Louhimo, I. Sawczuk, K. Taketa and E. P. Diamandis (2010). USE OF TUMOR MARKERS IN LIVER, BLADDER, CERVICAL, AND GASTRIC CANCERS, The National Academy of Clinical Biochemistry. PDF
- Sturgeon, C. M., B. R. Hoffman, D. W. Chan, S. L. Ch’ng, E. Hammond, D. F. Hayes, L. A. Liotta, E. F. Petricoin, M. Schmitt, O. J. Semmes, G. Soletormos, E. van der Merwe, E. P. Diamandis and B. National Academy of Clinical (2008). “National Academy of Clinical Biochemistry Laboratory Medicine Practice Guidelines for use of tumor markers in clinical practice: quality requirements.” Clin Chem 54(8): e1-e10. DOI: 10.1373/clinchem.2007.094144
- Trape, J., G. Gurt, J. Franquesa, J. Montesinos, A. Arnau, M. Sala, F. Sant, E. Casado, J. M. Ordeig, C. Bergos, F. Vida, P. Sort, A. Isava, M. Gonzalez and R. Molina (2015). “Diagnostic Accuracy of Tumor Markers CYFRA21-1 and CA125 in the Differential Diagnosis of Ascites.” Anticancer Res 35(10): 5655-5660. PMID: 26408739
- Trape, J., R. Molina, F. Sant, J. Montesinos, A. Arnau, J. Franquesa, R. Blavia, E. Martin, E. Marquilles, D. Perich, C. Perez, J. M. Roca, M. Domenech, J. Lopez and J. M. Badal (2012). “Diagnostic accuracy of tumour markers in serous effusions: a validation study.” Tumour Biol 33(5): 1661-1668. DOI: 10.1007/s13277-012-0422-3
- Trapé Pujol, J. and R. Molina Porto (2006). “Aspectos generales de los marcadores tumorales.” JANO 1620: 45-48. PDF

